Coronavirus: EE.UU. no aprueba por ahora el tratamiento con plasma

WASHINGTON.- La semana pasada, justo cuando la Administración de Alimentos y Medicamentos (FDA, según sus siglas en inglés) de Estados Unidos se estabapreparando para emitir una autorización de emergencia para el plasma sanguíneo como tratamiento del Covid-19, un grupo de altos funcionarios de salud federales intervino, argumentando que los datos emergentes sobre el tratamiento eran demasiado débiles, según dos altos funcionarios de la administración, de acuerdo con The New York Times.
La autorización está en espera por ahora mientras se revisan más datos, según H. Clifford Lane, director clínico del Instituto Nacional de Alergias y Enfermedades Infecciosas. Aún se podría emitir una aprobación de emergencia en un futuro cercano, dijo.
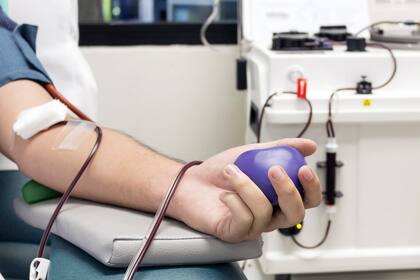
Donado por personas que han sobrevivido a la enfermedad, el plasma rico en anticuerpos se considera seguro. El presidente norteamericano Donald Trump lo ha aclamado como un "ingrediente hermoso" en las venas de las personas que han sobrevivido al Covid-19.
Pero los ensayos clínicos no han demostrado si el plasma puede ayudar a las personas a combatir el coronavirus.
Varios altos funcionarios de salud, dirigidos por Francis Collins, director de los Institutos Nacionales de Salud; Anthony Fauci, el principal experto en enfermedades infecciosas del gobierno; y Clifford Lane - instaron a sus colegas la semana pasada a esperar, citando datos recientes del estudio de plasma más grande del país, realizado por la Clínica Mayo. Pensaron que los datos del estudio hasta la fecha no eran lo suficientemente sólidos como para justificar una aprobación de emergencia.
"Los tres estamos bastante alineados en la importancia de contar con datos sólidos a través de ensayos de control aleatorios, y creemos que una pandemia no cambia eso", dijo Lane en una entrevista el martes pasado.
La autorización de emergencia redactada se basó en el historial del uso de plasma en otros brotes de enfermedades y en la investigación con animales y una serie de estudios de plasma, incluido el programa de la Clínica Mayo, que ha administrado infusiones a más de 66.000 pacientes con Covid-19 gracias al financiamiento del gobierno federal.
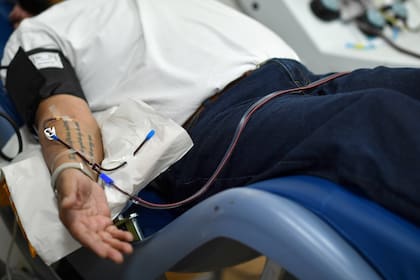
Trump reaccionó con enojo, sugiriendo que la decisión tenía motivaciones políticas. "Hay mucha gente allí que no quiere apresurar las cosas porque quieren hacerlo después del 3 de noviembre", dijo refiriéndose al día de las elecciones, mientras proclamó sin evidencia que el plasma convaleciente ayudó "más del 50 por ciento". de pacientes con Covid-19.
El plasma, el líquido amarillo pálido que queda después de que la sangre es despojada de sus glóbulos rojos y blancos, ha sido objeto de meses de intenso entusiasmo por parte de científicos, celebridades y Trump, mientras las compañías farmacéuticas siguen en carrera para completar docenas de ensayos clínicos para vacunas contra el coronavirus.
La autorizaciones de emergencia, que no requieren el mismo nivel de evidencia la aprobación de la FDA, fueron un tema delicado para el gobierno durante la pandemia. La agencia dio una autorización de emergencia a la hidroxicloroquina y cloroquina, que se usan para la malaria, pero tuvo que rescindirla meses después, luego de que se descubrió que los medicamentos eran ineficaces contra el coronavirus y potencialmente dañinos.
Los altos funcionarios de salud han expresado en privado su preocupación por el rápido crecimiento del programa de la Clínica Mayo y la prisa percibida por declarar que el plasma es efectivo sin la afirmación de los resultados de ensayos aleatorios, en los que los científicos han confiado durante mucho tiempo como el estándar de oro de la evidencia. El aumento vertiginoso de las inscripciones en el programa ha provocado un debate entre los investigadores sobre qué tipo de certeza empírica se necesita para tratar a los pacientes en una emergencia de salud pública.
Otras noticias de Actualidad
 1
1El chavismo afirma que el opositor que dejó la embajada argentina colabora activamente con la Justicia
 2
2The Economist nombró al país del año: cuál fue el elegido y qué dijo sobre la Argentina
- 3
Un ómnibus chocó con un camión y se prendió fuego: 32 muertos
 4
4Cómo el caso Pelicot relanzó debates jurídicos y sociales y qué podría cambiar tras la sentencia en Francia





